Iklan
Iklan
Pertanyaan
Sebanyak 100 mL larutan mengandung HCOOH dan HCOONa masing-masing 0,1 M ( Ka = 1 0 − 5 ) Hitung pH larutan awal Hitung pH setelah ditambah 1 mL HCl 0,1 M (tulis reaksi yang terjadi) Hitung pH setelah ditambah 1 mL NaOH 0,1 M (tulis reaksi yang terjadi)
Sebanyak 100 mL larutan mengandung HCOOH dan HCOONa masing-masing 0,1 M
- Hitung pH larutan awal
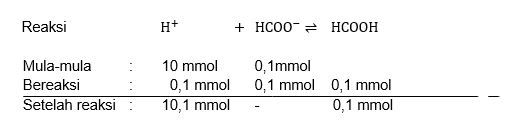
- Hitung pH setelah ditambah 1 mL HCl 0,1 M (tulis reaksi yang terjadi)
- Hitung pH setelah ditambah 1 mL NaOH 0,1 M (tulis reaksi yang terjadi)
Iklan
RH
R. Harmiasri
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
11
4.3 (6 rating)
Iklan
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2024 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia