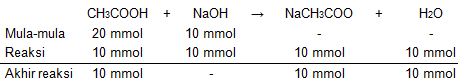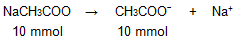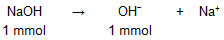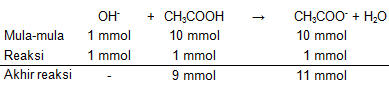pH larutan penyangga setelah dimasukkan NaOHtambahan adalah 4,79.
Asam asetat (CH3COOH) merupakan asam lemah, sedangkan natrium hidroksida (NaOH) merupakan basa kuat. Campuran antara asam lemah dengan basa kuat akan membentuk larutan penyangga asam jika asam lemah sisa.
Untuk mengetahui pH campuran 100 mL CH3COOH 0,2 M dengan 100 mL larutan NaOH 0,1 M yang kemudian ditambahkan 10 mL NaOH 0,1 M, perlu dihitung dengan cara berikut:
1. Menentukan mol mula-mula CH3COOH, NaOHawal, dan NaOHtambahan
mol CH3COOHmol NaOHawalmol NaOHtambahan =========[CH3COOH]×volume CH3COOH0,2 M×100 mL20 mmol[NaOH]awal×volume NaOHawal0,1 M×100 mL10 mmol[NaOH]tambahan×volume NaOHtambahan0,1 M×10 mL1 mmol
2. Menentukan mol basa konjugasi  sebelum dimasukkan NaOHtambahan
sebelum dimasukkan NaOHtambahan
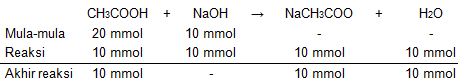
Dari tabel di atas, mol CH3COOH sisa adalah 10 mmol dan mol NaCH3COO yang terbentuk adalah 10 mmol, sehingga mol basa konjugasinya dapat dihitung sebagai berikut:
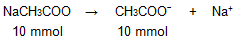
Dari persamaan reaksi di atas, dapat diketahui bahwa koefisien NaCH3COO sama dengan koefisien CH3COO−, sehingga mol NaCH3COO sama dengan mol CH3COO−, yaitu 10 mmol.
3. Menentukan mol basa konjugasi  setelah dimasukkan NaOHtambahan
setelah dimasukkan NaOHtambahan
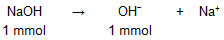
1 mmol ion OH− dari NaOH yang ditambahkan ke larutan penyangga akan bereaksi dengan 10 mmol CH3COOH sisa, sehingga mol basa konjugasi CH3COO− akan bertambah.
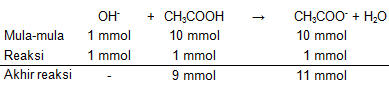
Dari tabel di atas, mol CH3COOH sisa setelah diberi NaOHtambahan adalah 9 mmol dan mol CH3COO− akhir yang terbentuk adalah 11 mmol.
4. Menentukan konsentrasi ion  setelah dimasukkan NaOHtambahan
setelah dimasukkan NaOHtambahan
[H+]===Ka×mol CH3COO−mol CH3COOH sisa1,8×10−5 M×11 mmol9 mmol1,62×10−5 M
5. Menentukan pH campuran setelah dimasukkan NaOHtambahan
pH====−log [H+]−log (1,62×10−5)5−log 1,624,79
Dari perhitungan di atas, dapat diketahui bahwa pH larutan penyangga setelah dimasukkan NaOHtambahan adalah 4,79.