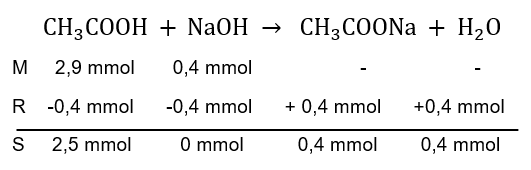Iklan
Pertanyaan
Sebanyak 29 mL larutan 0,1 M CH 3 COOH ( K a = 1 , 6 X 1 0 − 5 ) dicampurkan dengan 8 mL larutan 0,05 M NaOH dan diencerkan dengan air hingga volumenya menjadi 100 mL. pH larutan yang terbentuk adalah ...
Sebanyak 29 mL larutan 0,1 M dicampurkan dengan 8 mL larutan 0,05 M dan diencerkan dengan air hingga volumenya menjadi 100 mL. pH larutan yang terbentuk adalah ...
3
4
5
6
8
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
13
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia