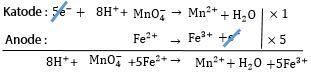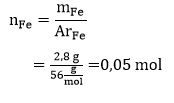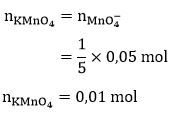Iklan
Pertanyaan
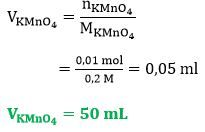
Besi sebanyak 2,8 gram dilarutkan dalam larutan asam sehingga membentuk ion Fe 2 + .Larutan tersebut lalu direaksikan dengan larutan KMnO 4 0,2 M menurut reaksi: Fe 2 + + MnO 4 − → Fe 3 + + Mn 2 + ( belum setara ) Tentukan volume larutan yang digunakan! ( A r Fe = 56 g mol − 1 )
Besi sebanyak 2,8 gram dilarutkan dalam larutan asam sehingga membentuk ion . Larutan tersebut lalu direaksikan dengan larutan 0,2 M menurut reaksi:
Tentukan volume larutan yang digunakan!
Iklan
SL
S. Lubis
Master Teacher
Jawaban terverifikasi
2
3.0 (2 rating)
RH
RACHMAT HABIBI ASNAN
Jawaban tidak sesuai
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia