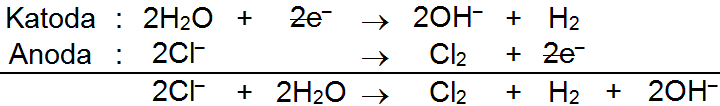Elektrolisis adalah reaksi redoks yang tidak bisa berlangsung spontan. Sel elektrolisis menggunakan listrik untuk melangsungkan reaksinya. Hal ini kebalikan dari sel Volta yang berlangsung spontan dan menghasilkan energi listrik. Pada sel elektrolisis katode bermuatan negatif dan anode bermuatan positif. Reaksi yang terjadi sama seperti pada sel Volta, yaitu reaksi reduksi pada katode dan reaksi oksidasi pada anode. Elektron mengalir memasuki larutan melalui kutub negatif (katode).
Untuk dapat menjawab soal di atas, maka terlebih dahulu perlu dibuat persamaan reaksi elektrolisisnya. Pada soal di atas, larutan  di elektrolisis dengan elektrode karbon yang merupakan elektroda inert, maka elektroda tidak ikut bereaksi dalam proses elektrolisis. Persamaan reaksi elektrolisis
di elektrolisis dengan elektrode karbon yang merupakan elektroda inert, maka elektroda tidak ikut bereaksi dalam proses elektrolisis. Persamaan reaksi elektrolisis  tersebut adalah sebagai berikut.
tersebut adalah sebagai berikut.
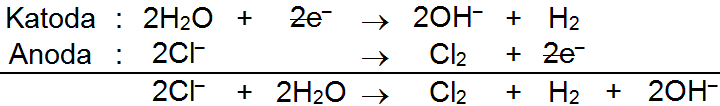
Pada persamaan reaksi elektrolisis di atas, ion  tidak mengalami reaksi reduksi karena Na merupakan logam golongan I A yang potensial elektrodanya lebih negatif daripada air, maka yang tereduksi adalah air. Ion
tidak mengalami reaksi reduksi karena Na merupakan logam golongan I A yang potensial elektrodanya lebih negatif daripada air, maka yang tereduksi adalah air. Ion  mengalami reaksi oksidasi pada anoda menjadi gas
mengalami reaksi oksidasi pada anoda menjadi gas  .
.
Selanjutnya volume gas  yang telah diketahui diubah menjadi mol terlebih dahulu, kemudian untuk mengetahui volume gas hidrogen, digunakan perbandingan koefisien antara gas klor (
yang telah diketahui diubah menjadi mol terlebih dahulu, kemudian untuk mengetahui volume gas hidrogen, digunakan perbandingan koefisien antara gas klor ( ) dengan gas hidrogen (
) dengan gas hidrogen ( ) pada persamaan reaksi elektrolisisnya. Jumlah mol dari 1,12 liter gas
) pada persamaan reaksi elektrolisisnya. Jumlah mol dari 1,12 liter gas  pada STP adalah sebagai berikut.
pada STP adalah sebagai berikut.

Pada reaksi elektrolisis larutan  di atas, diketahui bahwa koefisien reaksi gas
di atas, diketahui bahwa koefisien reaksi gas  = koefisien reaksi gas
= koefisien reaksi gas  , yaitu sama dengan 1, maka jumlah mol gas
, yaitu sama dengan 1, maka jumlah mol gas  = mol gas
= mol gas  . Volume gas
. Volume gas  yang terbentuk di katoda jika diukur pada keadaan STP adalah sebagai berikut.
yang terbentuk di katoda jika diukur pada keadaan STP adalah sebagai berikut.

Dengan demikian, maka volume gas hidrogen yang terjadi di katoda diukur pada keadaan STP sama dengan volume gas klor, yaitu 1,12 L.
Jadi, jawaban yang tepat adalah B.