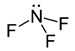Iklan
Pertanyaan
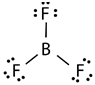
Molekul BF 3 dan NF 3 merupakan senyawa kovalen, tetapi BF 3 bersifat nonpolar sedangkan NF 3 bersifat polar. Hal ini disebabkan oleh . … Normal 0 false false false EN-US JA X-NONE /* Style Definitions */ table.MsoNormalTable {mso-style-name:"Table Normal"; mso-tstyle-rowband-size:0; mso-tstyle-colband-size:0; mso-style-noshow:yes; mso-style-priority:99; mso-style-parent:""; mso-padding-alt:0in 5.4pt 0in 5.4pt; mso-para-margin-top:0in; mso-para-margin-right:0in; mso-para-margin-bottom:8.0pt; mso-para-margin-left:0in; line-height:107%; mso-pagination:widow-orphan; font-size:11.0pt; font-family:"Calibri","sans-serif"; mso-ascii-font-family:Calibri; mso-ascii-theme-font:minor-latin; mso-hansi-font-family:Calibri; mso-hansi-theme-font:minor-latin; mso-bidi-font-family:"Times New Roman"; mso-bidi-theme-font:minor-bidi; mso-fareast-language:JA;}
Molekul BF3 dan NF3 merupakan senyawa kovalen, tetapi BF3 bersifat nonpolar sedangkan NF3 bersifat polar. Hal ini disebabkan oleh.…
keduanya isoelektronik
ukuran atom boron lebih besar dari nitrogen
boron termasuk logam dan nitrogen adalah gas
ikatan B-F bersifat nonpolar sedangkan ikatan N-F bersifat polar
BF3 berbentuk planar dan NF3 berbentuk piramida
Iklan
I. Solichah
Master Teacher
2
2.6 (6 rating)
flyzq
Bantu banget Makasih ❤️ Mudah dimengerti
nathan eben
ndak jelas ndak ada jawaban
Raydantio Dzikra
Pembahasan tidak menjawab soal
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia