Iklan
Pertanyaan
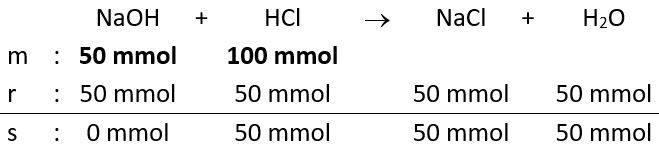
Diketahui persamaan termokimia reaksi neutralisasi asam klorida oleh natrium hidroksida sebagai berikut. HCl ( a q ) + NaOH ( a q ) → NaCl ( a q ) + H 2 O ( l ) △ H = − 54 kJ Hitung perubahan suhu yang akan terjadi jika 50 mL larutan NaOH 1 M direaksikan dengan 50 mL larutan HCl 2 M. Massa jenis dan kalor jenis larutan dapat dianggap sama dengan massa jenis dan kalor jenis air.
Diketahui persamaan termokimia reaksi neutralisasi asam klorida oleh natrium hidroksida sebagai berikut.
Hitung perubahan suhu yang akan terjadi jika 50 mL larutan 1 M direaksikan dengan 50 mL larutan 2 M. Massa jenis dan kalor jenis larutan dapat dianggap sama dengan massa jenis dan kalor jenis air.
Iklan
AM
A. Mulfi
Master Teacher
Mahasiswa/Alumni Institut Pertanian Bogor
Jawaban terverifikasi
1
5.0 (3 rating)
DS
Denia Situngkir
Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia