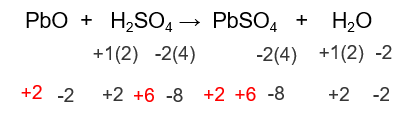Iklan
Pertanyaan
Tentukan apakah reaksi di bawah ini termasuk reaksi redoks atau bukan redoks? Jika termasuk reaksi redoks tentukan pula zat yang bertindak sebagai oksidator, zat yang bertindak sebagai reduktor, zat yang merupakan hasil reduksi, dan zat yang merupakan hasil oksidasi! PbO + H 2 SO 4 → PbSO 2 + H 2 O
Tentukan apakah reaksi di bawah ini termasuk reaksi redoks atau bukan redoks? Jika termasuk reaksi redoks tentukan pula zat yang bertindak sebagai oksidator, zat yang bertindak sebagai reduktor, zat yang merupakan hasil reduksi, dan zat yang merupakan hasil oksidasi!
Iklan
SL
S. Lubis
Master Teacher
Jawaban terverifikasi
1
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia