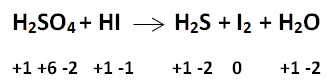Langkah pertama tentukan biloks masing-masing spesi tiap senyawa.
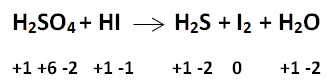
Atom S mengalami reduksi karena terjadi penurunan bilangan oksidasi sedangkan atom I mengalami oksidasi karena terjadi kenaikan bilangan oksidasi. Penyetaraan reaksi redoks dapat menggunakan metoda setengah sel. Reaksi oksidasi dan reduksi dipisah dalam penyetaraan ini.
- Reaksi reduksi atom

Tuliskan reaksi setengah sel reduksi  .
.

Kalikan koefisien reaksi  dengan 4 untuk menyetarakan jumlah atom oksigen. Kemudian tambahkan 8 ion
dengan 4 untuk menyetarakan jumlah atom oksigen. Kemudian tambahkan 8 ion  di ruas kiri untuk menyamakan jumlah atom hidrogen. Terakhir, tambahkan 8 elektron di sebelah kiri untuk menyamakan muatan di kedua ruas.
di ruas kiri untuk menyamakan jumlah atom hidrogen. Terakhir, tambahkan 8 elektron di sebelah kiri untuk menyamakan muatan di kedua ruas.

Tuliskan reaksi setengah sel reaksi oksidasi HI.

HI dikalikan dengan 2 untuk menyamakan jumlah atom I kedua ruas. Tambahkan 2 ion  di sebelah kanan untuk menyamakan jumlah atom hidrogen. Terakhir, tambahkan dua elektron untuk menyetarakan muatan kedua ruas.
di sebelah kanan untuk menyamakan jumlah atom hidrogen. Terakhir, tambahkan dua elektron untuk menyetarakan muatan kedua ruas.

- Penyetaraan dan eliminasi jumlah elektron
Untuk menyamakan jumlah elektron sehingga dapat dieliminasi maka kedua reaksi perlu dikalikan dengan bilangan tertentu. Persamaan reaksi reduksi dapat dikalikan dengan 1 sedangkan reaksi oksidasi dikalikan dengan 4 agar elektron dapat dikalikan.

Dengan demikian, reaksi redoks yang setara untuk soal di atas adalah  .
.
Jadi, jawaban yang benar adalah
 .
.