Iklan
Pertanyaan
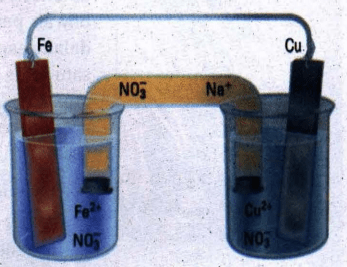
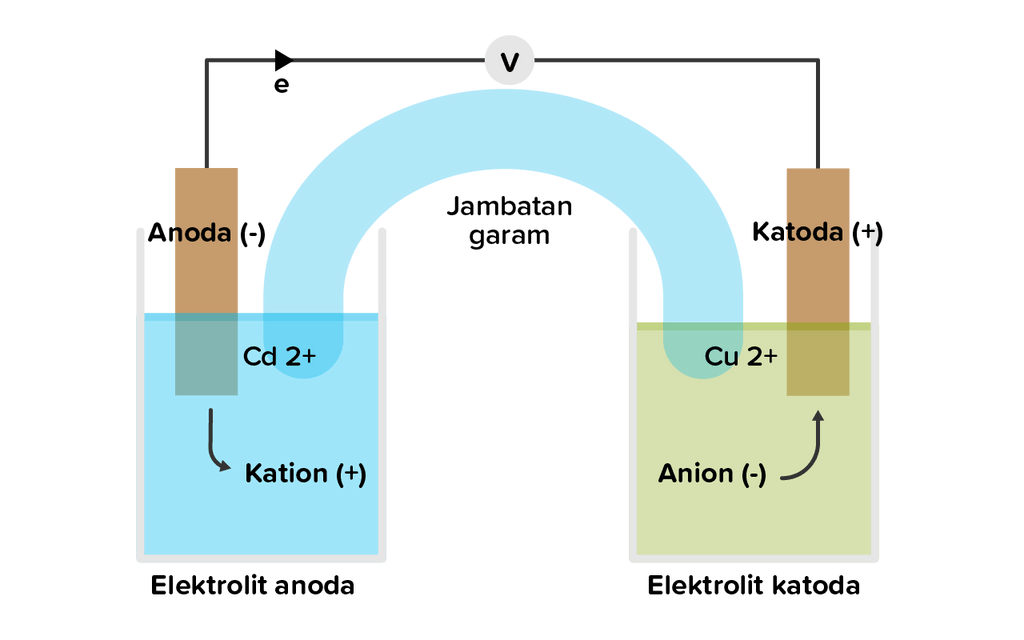
Sel Volta sederhana tersusun atas Fe ( s ) dan Fe ( NO 3 ) 2 ( a q ) dalam suatu wadah dan Cu ( s ) dan Cu ( NO 3 ) 2 ( a q ) dalam wadah lainnya. Sebuah kabel menghubungkan kedua elektrode dan jembatan garam yang mengandung NaNO 3 menghubungkan kedua larutan dalam wadah. Reaksi keseluruhannya adalah Fe ( s ) + Cu 2 + ( a q ) → Cu ( s ) + Fe 2 + ( a q ) A. Reaksi apa yang terjadi pada anode? B. Reaksi apa yang terjadi pada katode? C. Ke mana arah aliran elektron pada kabel luar? D. Ke manah arah aliran ion dalam jembatan garam? E. Gambarkan diagram selnya dengan melengkapi anode, katode, arah aliran elektron, dan arah aliran ion.
Sel Volta sederhana tersusun atas dan dalam suatu wadah dan dan dalam wadah lainnya. Sebuah kabel menghubungkan kedua elektrode dan jembatan garam yang mengandung menghubungkan kedua larutan dalam wadah. Reaksi keseluruhannya adalah
A. Reaksi apa yang terjadi pada anode?
B. Reaksi apa yang terjadi pada katode?
C. Ke mana arah aliran elektron pada kabel luar?
D. Ke manah arah aliran ion dalam jembatan garam?
E. Gambarkan diagram selnya dengan melengkapi anode, katode, arah aliran elektron, dan arah aliran ion.
Iklan
I. Yassa
Master Teacher
7
4.6 (6 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia