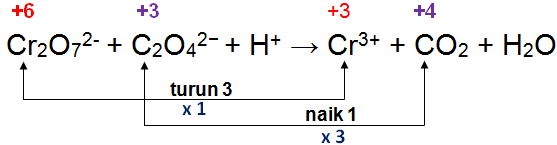Cara penyetaraan persamaan reaksi redoks dapat dilakukan dengan dua cara, yaitu cara setengah reaksi dan cara perubahan bilangan oksidasi. Cara penyetaraan persamaan reaksi redoks dengan cara setengah reaksi yaitu dengan melihat elektron yang diterima atau dilepaskan. Penyetaraan dilakukan dengan menyamakan jumlah elektronnya. Cara ini diutamakan untuk reaksi dengan suasana reaksi telah diketahui. Cara penyetaraan persamaan reaksi dengan cara perubahan bilangan oksidasi yaitu dengan cara melihat perubahan bilangan oksidasinya. Penyetaraan dilakukan dengan menyamakan perubahan bilangan oksidasi.
Langkah-langkah penyetaraan persamaan reaksi di atas adalah sebagai berikut.
- Menentukan perubahan bilangan oksidasi dan menyamakan perubahan bilangan oksidasinya.

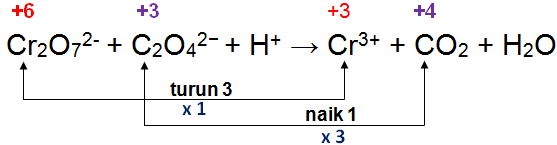
Pada persamaan reaksi di atas, atom C mengalami kenaikan biloks sebanyak 1, sedangkan atom Cr mengalami penurunan biloks sebanyak 3. Untuk menyamakan perubahan biloks keduanya, maka pada reaksi oksidasi reaksinya dikalikan 3, sedangkan pada reaksi reduksi reaksinya dikalikan 1 agar jumlah perubahan biloksnya sama dengan 3.
- Menyamakan koefisien unsur-unsur yang mengalami perubahan bilangan oksidasi.

Pada persamaan reaksi di atas, diketahui jumlah atom Cr di ruas kiri = 2, sedangkan jumlah Cr di ruas kanan = 1, maka pada ion  diberi koefisien 2. Jumlah atom C di ruas kiri = 2, sedangkan jumlah atom C di ruas kanan = 1, maka pada senyawa
diberi koefisien 2. Jumlah atom C di ruas kiri = 2, sedangkan jumlah atom C di ruas kanan = 1, maka pada senyawa  diberi koefisien 2. Persamaan reaksinya akan menjadi seperti berikut.
diberi koefisien 2. Persamaan reaksinya akan menjadi seperti berikut.

- Memberikan koefisien reaksi pada reaksi oksidasi dan reduksi sesuai angka pengalinya.

Untuk menyamakan perubahan biloks pada reaksi reduksi dan oksidasi, maka pada reaksi oksidasi koefisien reaksinya dikalikan 3, sedangkan pada reaksi reduksi koefisien reaksinya dikalikan 1. Dengan demikian, maka persamaan reaksinya menjadi seperti berikut.

- Menyamakan jumlah muatan pada kedua ruas persamaan reaksi.

Untuk menyamakan jumlah muatan di ruas kiri kanan, dilakukan dengan menambahkan koefisien di depan ion  . Jumlah muatan pada ruas kiri adalah -8, sedangkan muatan di ruas kanan adalah +6, maka ditambahkan koefisien 14 di depan ion
. Jumlah muatan pada ruas kiri adalah -8, sedangkan muatan di ruas kanan adalah +6, maka ditambahkan koefisien 14 di depan ion  . Persamaan reaksi yang telah disetarakan muatannya adalah sebagai berikut.
. Persamaan reaksi yang telah disetarakan muatannya adalah sebagai berikut.

- Menyamakan jumlah atom hidrogen di kedua ruas.

Jumlah atom H di ruas kiri = 14, dan jumlah atom H di ruas kanan = 2. Jadi jumlah atom H di ruas kanan perlu ditambahkan dengan memberi koefisien 7 pada senyawa  . Persamaan reaksi setaranya adalah sebagai berikut.
. Persamaan reaksi setaranya adalah sebagai berikut.

Setelah persamaan reaksi disetarakan, nilai a = 1, b = 3, c = 14, d = 2, e = 6, dan f = 7. Dengan demikian, nilai a, b, d, e berturut-turut 1, 3, 2, dan 6.
Jadi, jawaban yang tepat adalah B.