Iklan
Pertanyaan
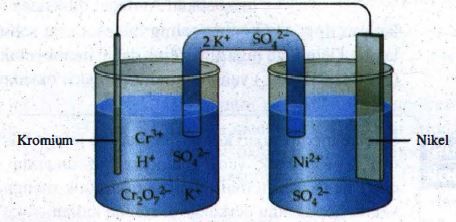
Perhatikan sel Volta berikut. A. Ke arahmana elektron mengalir melalui rangkaian eksternal? B. Setengah sel mana yang mengalami oksidasi? C. Setengah sel mana elektron masuk ke dalam sel? D. Elektrode mana yang menerima elektron? E. Elektrode mana yang bermuatan negatif?
Perhatikan sel Volta berikut.
A. Ke arah mana elektron mengalir melalui rangkaian eksternal?
B. Setengah sel mana yang mengalami oksidasi?
C. Setengah sel mana elektron masuk ke dalam sel?
D. Elektrode mana yang menerima elektron?
E. Elektrode mana yang bermuatan negatif?
Iklan
GS
G. Suprobo
Master Teacher
Mahasiswa/Alumni Institut Pertanian Bogor
Jawaban terverifikasi
4
4.7 (13 rating)
SA
Shalmayra Alya Qonita
Ini yang aku cari! Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia