Iklan
Pertanyaan
Perhatikan sel elektrolisis di bawah ini: Jika arus listrik yang digunakan sebesar 5 ampere dan endapan yang terbentuk 1,18 gram. ( A r Cu = 63 , 5 dan Cl = 35 , 5 ) Tulislah reaksi elektrolisis leburan CuCl 2 ! Hitunglah waktu yang digunakan selama elektrolisis!
Perhatikan sel elektrolisis di bawah ini:
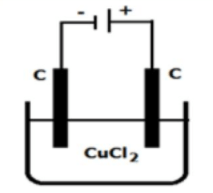
Jika arus listrik yang digunakan sebesar 5 ampere dan endapan yang terbentuk 1,18 gram.
- Tulislah reaksi elektrolisis leburan !
- Hitunglah waktu yang digunakan selama elektrolisis!
Iklan
MD
M. Darry
Master Teacher
Mahasiswa/Alumni Universitas Indonesia
Jawaban terverifikasi
2
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia















