Iklan
Pertanyaan
Aluminium diketahui merupakan logam dengan penggunaan terbanyak kedua dl dunia setelah besi atau baja. Logam aluminium merupakan logam yang ringan dengan bobot jenis . Meskipun ringan, logam aluminium termasuk logam yang kuat terutama apabila dipadukan dengan logam lain menghasilkan alloy seperti duralium (AI, Cu, Mg). Selain itu logam aluminium tahan korosi, tidak beracun, dan memilikin sifat konduktivitas yang tinggi. Sumber utama aluminium yang ada di alam berasal dari mineral bauksit
. Mineral bauksit mengandung 40-60% alumina
. Proses pembuatan aluminium dikenal sebagai proses bayer dan proses Hall-Heroult. Proser bayer merupakan tahap ekstraksi alumina dari bijih bauksit. Sedangkan pada proses Hall-Heroult aluminium hidroksida dileburkan menjadi aluminium murni. Reaksi yang terjadi sebagai berikut:
Selanjutnya pada proses Hall-Heroult leburan dielektrolisis dengan menggunakan elektrode karbon pada suhu .
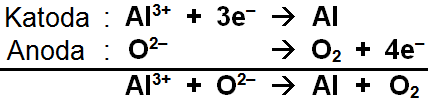
Pada elektrolisis yang dilakukan dengan mengalirkan arus listrik sebesar 10 A diperoleh logam Al yang mengendap di katode sebesar 9 gram. Laju pembentukan logam di katode adalah ...
Pada elektrolisis yang dilakukan dengan mengalirkan arus listrik sebesar 10 A diperoleh logam Al yang mengendap di katode sebesar 9 gram. Laju pembentukan logam di katode adalah ...
Iklan
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
1
5.0 (2 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia















