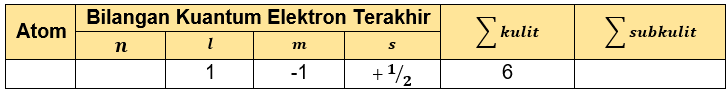
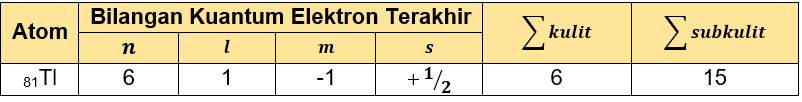
Tabel yang lengkap adalah sebagai berikut.
Konfigurasi elektron dan nama unsur dapat ditentukan dari keempat bilangan kuantum pada elektron terakhir. Keempat bilangan kuantum dapat disusun menjadi elektron terakhir dengan aturan:
- Bilangan kuantum utama (n), yang menunjukkan kulit atom.
- Bilangan kuantum azimuth (l), yang menunjukkan subkulit atom.
- Bilangan kuantum magnetik (m), yang menunjukkan orientasi orbital.
- Bilangan kuantum spin (s), yang menunjukkan arah rotasi elektron.
Berdasarkan keterangan tersebut, maka:
Bilangan kuantum utama
Bilangan kuantum utamanya adalah sama dengan jumlah kulit, n = 6
Elektron terakhirnya adalah:
Dengan n = 6, l = 1, m = -1, dan s = +21, maka dapat diketahui elektron terakhirnya ada pada subkulit 6p dengan jumlah elektron:
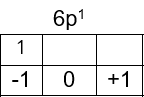
Konfigurasi elektronnya adalah: 1s22s22p63s23p64s23d104p65s24d105p66s24f145d106p1
Berdasarkan konfigurasi elektron, maka jumlah subkulitnya adalah 15.
Jumlah elektron dan unsurnya adalah:
Jumlah elektron 81, pada unsur netral, jumlah elektron sama dengan nomor atom. Unsur dengan nomor atom 81 pada sistem periodik unsur adalah 81Tl.
Sehingga tabel tersebut dapat dilengkapi: