Iklan
Pertanyaan
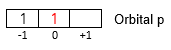
Electron terakhir suatu unsurmempunyai bilangan kuantum n = 3, ℓ = 1, m = 0, dan s = +1/2. Salah satu isotop unsuritu mempunyai neutron = 15. Nomor massa isotop tersebut adalah
Electron terakhir suatu unsur mempunyai bilangan kuantum n = 3, ℓ = 1, m = 0, dan s = +1/2. Salah satu isotop unsur itu mempunyai neutron = 15. Nomor massa isotop tersebut adalah
23
25
27
29
31
Iklan
SL
S. Lubis
Master Teacher
Mahasiswa/Alumni Universitas Sumatera Utara
Jawaban terverifikasi
1
4.6 (18 rating)
CO
Cece Odang
Ini yang aku cari! Bantu banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia