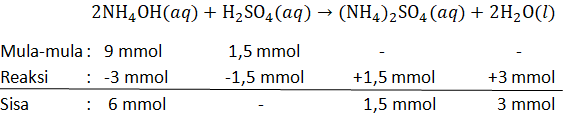Iklan
Pertanyaan
Ke dalam 90 mL larutan NH 4 OH 0,1M ( K b NH 4 OH = 1 0 − 5 ) dicampurkan dengan 15mL larutan H 2 SO 4 0,1M, makapH larutan yang terjadi adalah ...
Ke dalam 90 mL larutan 0,1 M dicampurkan dengan 15 mL larutan 0,1 M, maka pH larutan yang terjadi adalah ...
Iklan
BR
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
8
5.0 (2 rating)
Iklan
Pertanyaan serupa
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia