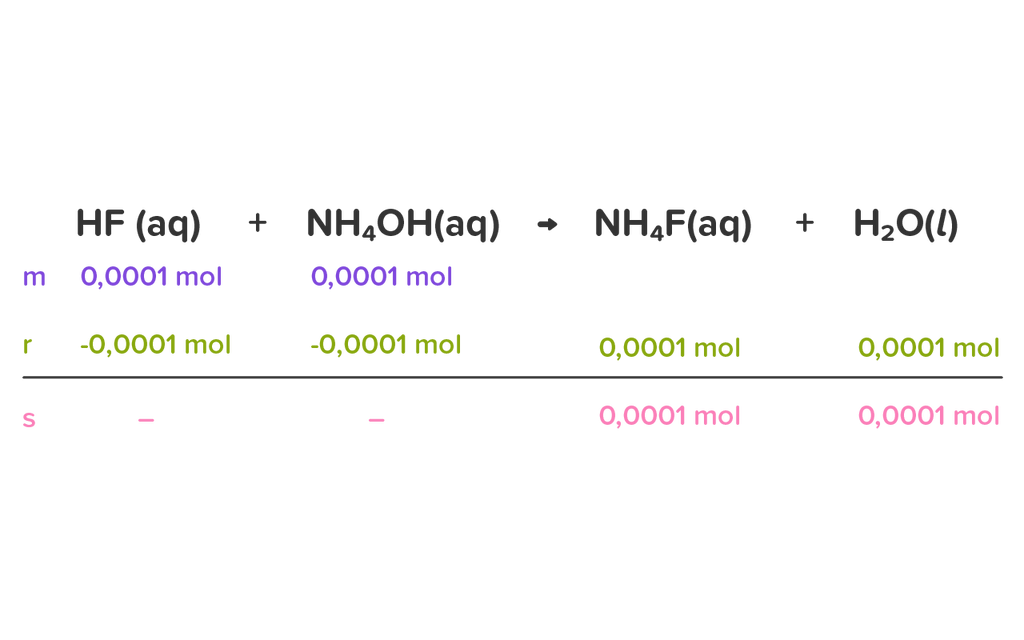Iklan
Pertanyaan
Hitunglah pH larutan dari : b. 100 mL HF 0,001 M dan 25 mL NH 4 OH 0,004 M ( Ka HF = 1 , 6 × 1 0 − 4 , Ka CH 3 COOH = 1 , 8 × 1 0 − 5 , dan Kb NH 4 OH = 1 × 1 0 − 5 )
Hitunglah pH larutan dari :
b. 100 mL HF 0,001 M dan 25 mL 0,004 M
Iklan
NP
N. Puspita
Master Teacher
Jawaban terverifikasi
2
4.7 (4 rating)
BH
Bunga Hasti
Makasih ❤️
RR
Rizar Radhiya Aqsa
Jawaban tidak sesuai
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia