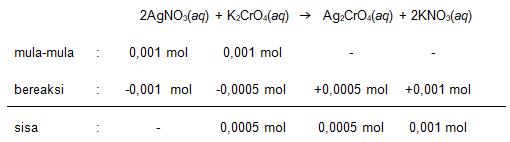Iklan
Pertanyaan
Diketahui hasil kali kelarutan perak kromat, Ag 2 CrO 4 = 3 , 0 × 1 0 − 12 L mol . Prediksikan apakah akan terbentuk endapan jika volume yang sama larutan 0,001 M AgNO 3 dicampurkan dengan larutan 0,001 M K 2 CrO 4 !
Diketahui hasil kali kelarutan perak kromat, . Prediksikan apakah akan terbentuk endapan jika volume yang sama larutan 0,001 M dicampurkan dengan larutan 0,001 M !
Iklan
SS
S. Susanti
Master Teacher
Mahasiswa/Alumni Universitas Jayabaya
Jawaban terverifikasi
1
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia