Iklan
Pertanyaan
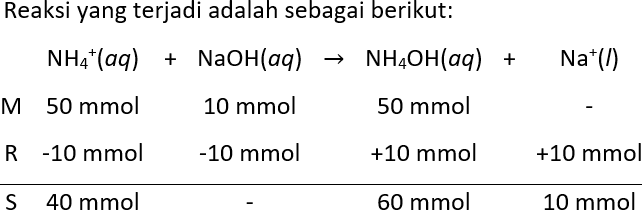
Diketahui campuran 500 mL larutan NH 4 OH 0,1 M dan 500 mL larutan NH 4 Cl 0,1 M. ( K b = 1 , 8 × 1 0 − 5 ) TentukanpH larutan setelah penambahan 50 mL NaOH 0,2 M.
Diketahui campuran 500 mL larutan 0,1 M dan 500 mL larutan 0,1 M. Tentukan pH larutan setelah penambahan 50 mL 0,2 M.
Iklan
BR
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
4
4.8 (5 rating)
W
Widi
Bantu banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia



 .
.











