Iklan
Pertanyaan
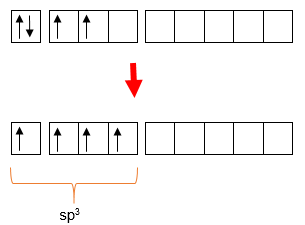
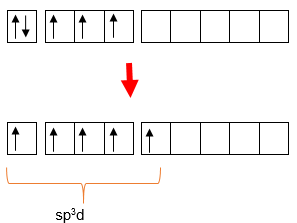
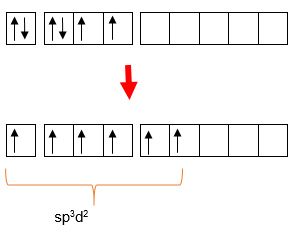
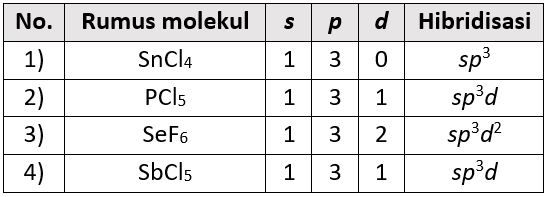
Diketahui beberapa molekul senyawa berikut. 1 ) SnCl 4 2 ) PCl 5 3 ) SeF 6 4 ) SbCl 5 Senyawa yang mempunyai orbital hibrida s p 3 d ditunjukkan oleh angka .... (Nomor atom: Sn = 50 , P = 15 , Se = 34 , Sb = 51 )
Diketahui beberapa molekul senyawa berikut.
Senyawa yang mempunyai orbital hibrida ditunjukkan oleh angka .... (Nomor atom: , , , )
1) dan 2)
1) dan 3)
1) dan 4)
2) dan 3)
2) dan 4)
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
1
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia