Cara penyetaraan persamaan reaksi redoks dapat dilakukan dengan dua cara, yaitu cara setengah reaksi dan cara perubahan bilangan oksidasi. Cara penyetaraan persamaan reaksi redoks dengan cara setengah reaksi yaitu dengan melihat elektron yang diterima atau dilepaskan. Penyetaraan dilakukan dengan menyamakan jumlah elektronnya. Cara ini diutamakan untuk reaksi dengan suasana reaksi telah diketahui. Cara penyetaraan persamaan reaksi dengan cara perubahan bilangan oksidasi, yaitu dengan cara melihat perubahan bilangan oksidasinya. Penyetaraan dilakukan dengan menyamakan perubahan bilangan oksidasi.
Langkah-langkah penyetaraan persamaan reaksi di atas adalah sebagai berikut.
- Menentukan perubahan bilangan oksidasi dan menyamakan perubahan bilangan oksidasinya.

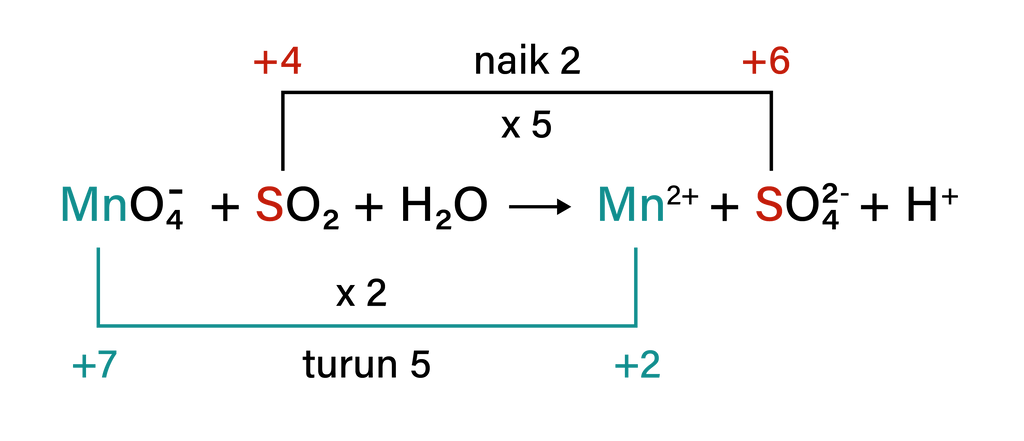
Pada reaksi di atas, diketahui bahwa atom Mn biloksnya naik sebesar 2, sedangkan atom S biloksnya turun sebesar 5. Untuk menyamakan jumlah perubahan biloksnya, pada reaksi oksidasi dikali 5 koefisiennya dan pada reaksi reduksi dikali 2 koefisiennya, agar total perubahan biloksnya menjadi 10.
- Menempatkan angka pengali pada tiap reaksi menjadi koefisien.

Pada reaksi oksidasi, koefisien reaksinya dikalikan 5 dan pada reaksi reduksi, koefisien reaksinya dikalikan 2, maka persamaan reaksinya menjadi seperti berikut.

- Menyamakan jumlah muatan di kedua ruas.

Untuk menyamakan jumlah muatan di ruas kiri kanan, dilakukan dengan menambahkan angka yang diperlukan di depan ion  . Pada soal di atas, muatan di ruas kiri adalah − 2, agar muatan di ruas kanan bernilai −2 juga, maka ditambahkan koefisien 4 di depan ion
. Pada soal di atas, muatan di ruas kiri adalah − 2, agar muatan di ruas kanan bernilai −2 juga, maka ditambahkan koefisien 4 di depan ion  . Setelah penambahan koefisien pada ion
. Setelah penambahan koefisien pada ion  , maka persamaan reaksi menjadi seperti berikut.
, maka persamaan reaksi menjadi seperti berikut.

- Menyamakan jumlah atom oksigen di kedua ruas.

Untuk menyamakan jumlah atom O di ruas kiri dan kanan, maka ditambahkan koefisien 2 didepan  . Dengan demikian, jumlah atom O di ruas kiri adalah 20, dan di ruas kanan juga sama dengan 20. Persamaan reaksi setaranya adalah sebagai berikut.
. Dengan demikian, jumlah atom O di ruas kiri adalah 20, dan di ruas kanan juga sama dengan 20. Persamaan reaksi setaranya adalah sebagai berikut.

Dengan demikian, maka nilai a = 2, nilai b = 5, nilai c = 2, nilai d = 2, nilai e = 5, dan nilai f = 4.
Jadi, nilai koefisien a, b, c, d, e, dan f berturut-turut adalah 2, 5, 2, 2, 5, dan 4.
















