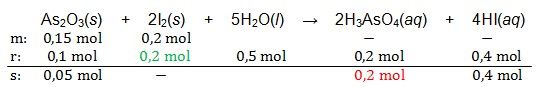Iklan
Pertanyaan
Asam arsenat dapat dihasilkan dari reaksi antara arsen trioksida dengan iod menurut reaksi berikut: As 2 O 3 ( s ) + I 2 ( s ) + H 2 O( l ) → H 3 AsO 4 ( aq ) + HI( aq ) (belum setara) Jika 29,7 gram arsen trioksida direaksikan dengan 50,8 gram iod dan air berlebih, massa asam arsenat yang dihasilkan adalah .... ( A r I = 127, As = 75, O = 16, H = 1)
Asam arsenat dapat dihasilkan dari reaksi antara arsen trioksida dengan iod menurut reaksi berikut:
As2O3(s) + I2(s) + H2O(l) → H3AsO4(aq) + HI(aq) (belum setara)
Jika 29,7 gram arsen trioksida direaksikan dengan 50,8 gram iod dan air berlebih, massa asam arsenat yang dihasilkan adalah .... (Ar I = 127, As = 75, O = 16, H = 1)
21,3 g
23,6 g
24,8 g
26,7 g
28,4 g
Iklan
JS
J. Siregar
Master Teacher
Mahasiswa/Alumni Universitas Negeri Medan
Jawaban terverifikasi
2
5.0 (3 rating)
MF
MELVIN FENDIPUTRA
Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia