Iklan
Pertanyaan
Indonesia kaya akan produksi apel khususnya di daerah Malang, Jawa Timur. Mengonsumsi apel hijau akan dapat meningkatkan kekebalan tubuh, mengurangi toksisitas, menambah energi, menyembuhkan penyakit hati dan gangguan otak dengan cara mengikat logam beracun dalam tubuh.
Khasiat apel hijau disebabkan kandungan asam malat yaitu asam dikarboksilat dengan rumus kimia . [Mr = 134 g/mol].
(sumber : http://www.amazine.co)
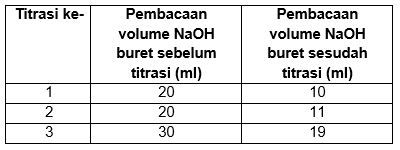
Untuk mengetahui kadar asam malat ditimbang sebuah apel dengan massa 75 gram lalu ditambahkan air sebanyak 100 ml kemudian diblender. Campuran disaring, filtrat yang diperoleh diambil 10 ml kemudian dititrasi sebanyak tiga kali dengan NaOH standar 0,1 M sampai mencapai titik akhir titrasi (hanya ada satu titik akhir titrasi) memerlukan volume NaOH yang tercantum pada data tabel berikut (indikator yang digunakan adalah PP). Hitung kadar asam malat dalam apel hijau (dinyatakan dalam % b/b) dan perubahan warna pada titik akhir titrasi yaitu....
Untuk mengetahui kadar asam malat ditimbang sebuah apel dengan massa 75 gram lalu ditambahkan air sebanyak 100 ml kemudian diblender. Campuran disaring, filtrat yang diperoleh diambil 10 ml kemudian dititrasi sebanyak tiga kali dengan NaOH standar 0,1 M sampai mencapai titik akhir titrasi (hanya ada satu titik akhir titrasi) memerlukan volume NaOH yang tercantum pada data tabel berikut (indikator yang digunakan adalah PP).
Hitung kadar asam malat dalam apel hijau (dinyatakan dalam % b/b) dan perubahan warna pada titik akhir titrasi yaitu....
0,0179%, dari tidak berwarna menjadi warna pink muda
0,179%, dari pink muda menjadi tidak berwarna
1,79%, dari tidak berwarna menjadi warna pink muda
1,79%, dari pink muda menjadi tidak berwarna
17,9%, dari tidak berwarna menjadi pink muda
Iklan
D. Zharva
Master Teacher
2
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia