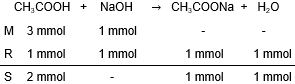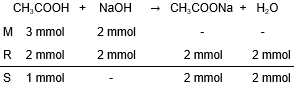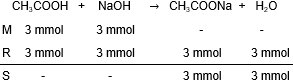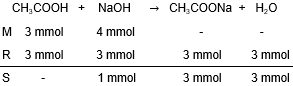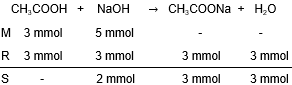Iklan
Pertanyaan
Sebanyak 15 mLasam cuka (CH 3 COOH) 0,2 M dititrasi dengan larutan NaOH 0,1 M. Hitunglah pH larutan dalam kondisi berikut. a. Sebelum ditambah NaOH b. Setelah ditambah NaOH sebanyak 10 mL c. Setelah ditambah NaOH sebanyak 20 mL d. Setelah ditambah NaOH sebanyak 30 mL e. Setelah ditambah NaOH sebanyak 40 mL f. Setelah ditambah NaOH sebanyak 50 mL Gambarkan kurva titrasi tersebut, tunjukkan titik ekuivalen dan daerah larutan penyangganya.
Sebanyak 15 mL asam cuka (CH3COOH) 0,2 M dititrasi dengan larutan NaOH 0,1 M. Hitunglah pH larutan dalam kondisi berikut.
a. Sebelum ditambah NaOH
b. Setelah ditambah NaOH sebanyak 10 mL
c. Setelah ditambah NaOH sebanyak 20 mL
d. Setelah ditambah NaOH sebanyak 30 mL
e. Setelah ditambah NaOH sebanyak 40 mL
f. Setelah ditambah NaOH sebanyak 50 mL
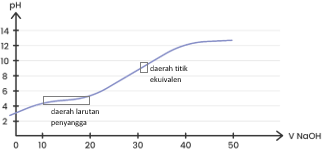
Gambarkan kurva titrasi tersebut, tunjukkan titik ekuivalen dan daerah larutan penyangganya.
Iklan
I. Nur
Master Teacher
Mahasiswa/Alumni Universitas Negeri Malang
4
4.5 (2 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia