Iklan
Pertanyaan
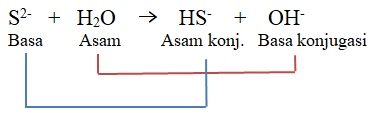
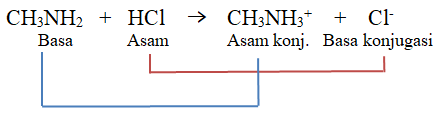
Tunjukkan pasangan asam-basa yang berkonjugasipada setiap reaksi berikut. a. S 2 − + H 2 O ⇄ HS − + OH − b. CH 3 NH 2 + HCl ⇄ CH 3 NH 3 + + Cl −
Tunjukkan pasangan asam-basa yang berkonjugasi pada setiap reaksi berikut.
a.
b.
Iklan
YS
Y. Sahara
Master Teacher
Mahasiswa/Alumni Universitas Negeri Malang
Jawaban terverifikasi
1
3.6 (3 rating)
NA
Nafill Amelia
Mudah dimengerti
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia