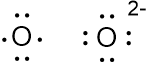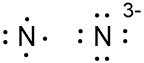Iklan
Pertanyaan
Tuliskan rumus lewis dari unsur non logam berikut 8 O , 17 Cl , 7 N , 6 C dan ramalkan kemungkinan ion yang dapat dibentuknya?
Tuliskan rumus lewis dari unsur non logam berikut dan ramalkan kemungkinan ion yang dapat dibentuknya?
Iklan
IN
I. Nur
Master Teacher
Mahasiswa/Alumni Universitas Negeri Malang
Jawaban terverifikasi
2
4.7 (8 rating)
N
NOVI
Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia