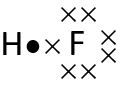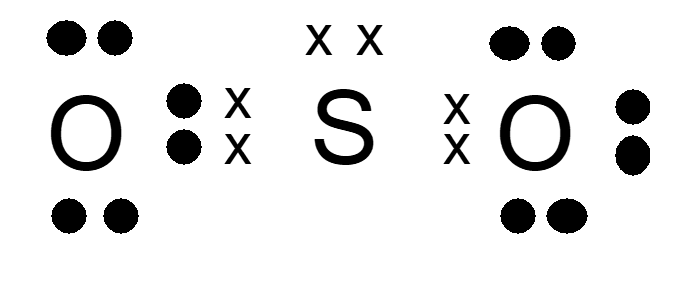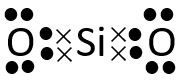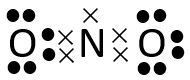Iklan
Pertanyaan
Di antara senyawa berikut yang mengalami penyimpangan kaidah oktet atau duplet adalah .... (Nomor atom: H = 1, O = 8, F = 9, Si = 14, C = 6, Cl = 17, N = 7, dan Be = 4)
Di antara senyawa berikut yang mengalami penyimpangan kaidah oktet atau duplet adalah .... (Nomor atom: H = 1, O = 8, F = 9, Si = 14, C = 6, Cl = 17, N = 7, dan Be = 4)
Iklan
UI
U. Ika
Master Teacher
Jawaban terverifikasi
3
4.5 (12 rating)
DM
Dree Minerva
Mudah dimengerti
AK
Alin Kogoya
Pembahasan tidak lengkap Pembahasan tidak menjawab soal
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia