Oksidator, reduktor, hasil oksidasi dan hasil reduksi pada reaksi SnCl2+I2+2HCl→SnCl4+2HI berturut-turut adalah I2; SnCl2; SnCl4; HI.
Pada penentuan bilangan oksidasi masing-masing unsur digunakan beberapa aturan biloks, diantaranya adalah:
- Biloks unsur logam golongan IA dan IIA dalam molekul masing-masing adalah +1 dan +2
- Biloks total molekul senyawa sama dengan nol (0)
- Biloks unsur bebas dan molekul unsur sama dengan nol (0)
- Biloks unsur F dalam molekul adalah -1
- Biloks unsur O dalam senyawa sama dengan -2, kecuali dalam senyawa peroksida, superoksida dan senyawa biner fluorida
- Biloks unsur unsur golongan VIIA dalam senyawa ion adalah -1
- Biloks H jika berikatan dengan nonlogam adalah +1
Pada reaksi redoks, zat di reaktan yang mengalami reaksi disebut dengan oksidator, sedangkan zat di reaktan yang mengalami oksidasi disebut dengan reduktor. Sedangkan di produk, zat yang menjadi hasil dari reaksi oksidasi disebut dengan hasil oksidasi dan zat yang menjadi hasil reaksi reduksi disebut dengan hasil reduksi. Biloks masing-masing unsur pada reaksi SnCl2+I2+2HCl→SnCl4+2HI adalah sebagai berikut
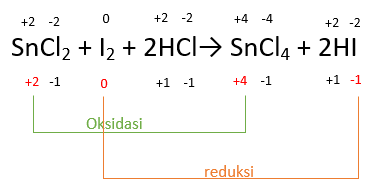
Biloks yang ada dibagian bawah adalah biloks dari satu buah unsur dalam senyawa, sedangkan biloks di bagian atas adalah biloks sejumlah unsur sesuai dengan jumlah unsur dalam senyawa tersebut. Gambar di atas memperlihatkan bahwa :
I2 adalah zat di reaktan yang mengalami penurunan biloks, maka I2 disebut sebagai oksidator.
SnCl2 adalah zat di reaktan yang mengalami kenaikan biloks, maka SnCl2 disebut sebagai reduktor.
SnCl4 adalah zat hasil reaksi oksidasi , maka SnCl4 disebut sebagai hasil oksidasi.
HI adalah zat hasil reaksi reduksi , maka HI disebut sebagaihasil reduksi.
Sehingga, Oksidator, reduktor, hasil oksidasi dan hasil reduksi pada reaksi SnCl2+I2+2HCl→SnCl4+2HI berturut-turut adalah I2; SnCl2; SnCl4; HI
















