Iklan
Pertanyaan
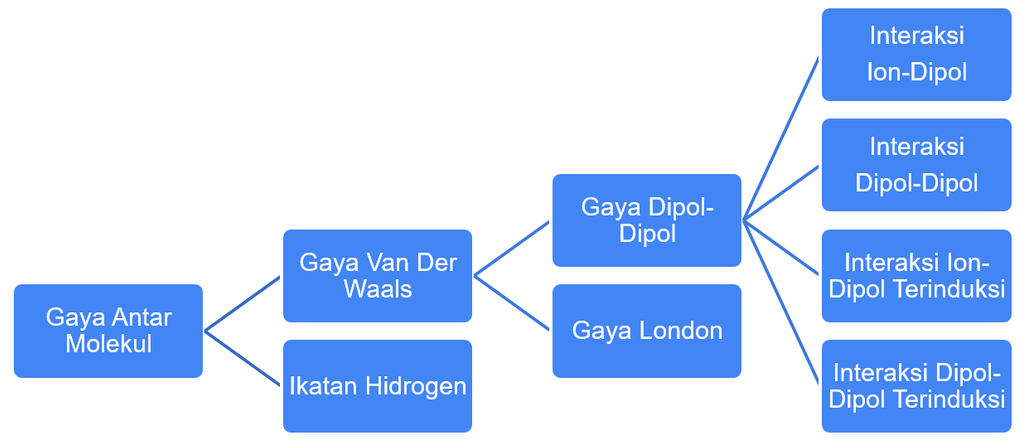
Tentukan gaya tarik-menarik antarmolekul apa saja yang terdapat dalam zat berikut! Karbon dioksida ( CO 2 ) Asam klorida ( HCl ) Air ( H 2 O )
Tentukan gaya tarik-menarik antarmolekul apa saja yang terdapat dalam zat berikut!
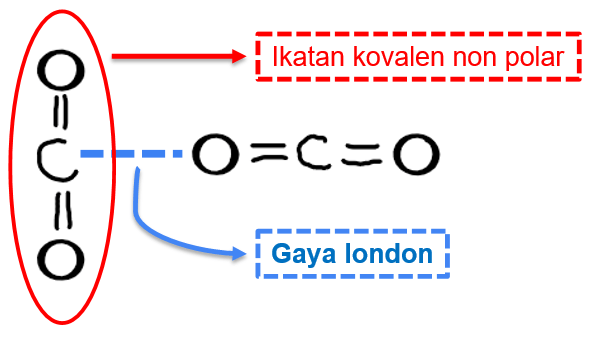
- Karbon dioksida
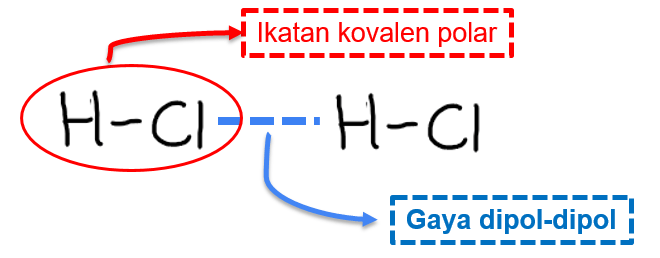
- Asam klorida
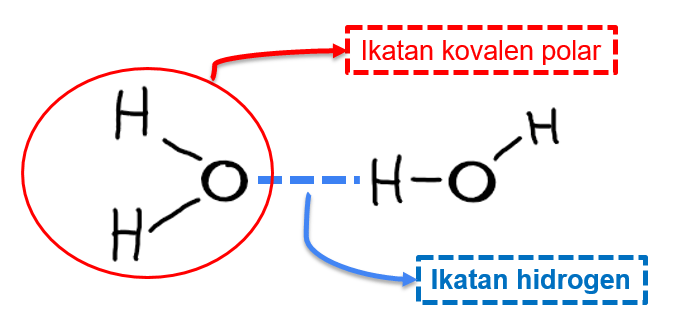
- Air
Iklan
NP
N. Puspita
Master Teacher
Jawaban terverifikasi
6
5.0 (4 rating)
MF
Meisha Fahriani Davela
Pembahasan lengkap banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia