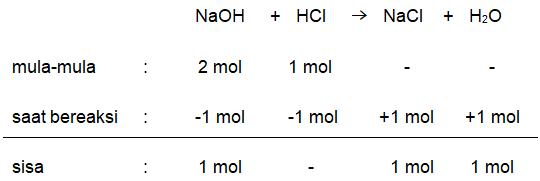Iklan
Pertanyaan
Sebanyak 80 gram NaOH direaksikan dengan 36,5 gram HCl menurut reaksi: NaOH + HCl → NaCl + H 2 O Jika Ar Na = 23, O = 16, H = 1, Cl = 35,5. Tentukan : a. Massa NaCl yang terbentuk b. Jumlah partikel air yang dihasilkan
Sebanyak 80 gram NaOH direaksikan dengan 36,5 gram HCl menurut reaksi:
Jika Ar Na = 23, O = 16, H = 1, Cl = 35,5. Tentukan :
a. Massa yang terbentuk
b. Jumlah partikel air yang dihasilkan
Iklan
SL
S. Lubis
Master Teacher
Jawaban terverifikasi
1
4.2 (5 rating)
IM
Irma Mardiana
Mudah dimengerti
HS
Hanun Shabrina
Pembahasan tidak menjawab soal
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia