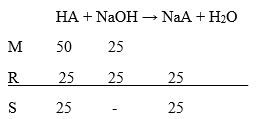Iklan
Pertanyaan
Sebanyak 100 ml larutan suatu asam lemah HA ( K a = 1 × 1 0 − 5 ) tepat bereaksi dengan 50 ml larutan KOH 0,2 M. Jika ke dalam 500 ml larutan asam tersebut ditambahkan 1 gram NaOH, pH larutan yang terbentuk adalah...(ArNa = 23, O= 16, dan H = 1)
Sebanyak 100 ml larutan suatu asam lemah HA tepat bereaksi dengan 50 ml larutan KOH 0,2 M. Jika ke dalam 500 ml larutan asam tersebut ditambahkan 1 gram NaOH, pH larutan yang terbentuk adalah... (Ar Na = 23, O = 16, dan H = 1)
1
2
3
4
5
Iklan
AM
A. Muhammad
Master Teacher
Mahasiswa/Alumni Universitas Pendidikan Indonesia
Jawaban terverifikasi
32
4.6 (10 rating)
KI
Kharisma Intania A
Makasih ❤️
HR
Hanari Rafina Azahra
Makasih ❤️ Ini yang aku cari! Bantu banget Pembahasan lengkap banget Mudah dimengerti
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia