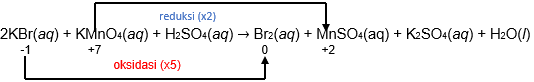Iklan
Pertanyaan
Reaksi setara pada persamaan reaksi: KBr ( a q ) + KMnO 4 ( a q ) + H 2 SO 4 ( a q ) → Br 2 ( a q ) + MnSO 4 ( a q ) + K 2 SO 4 ( a q ) + H 2 O ( l ) adalah ....
Reaksi setara pada persamaan reaksi: adalah ....
Iklan
MJ
M. Juliana
Master Teacher
Mahasiswa/Alumni Universitas Negeri Medan
Jawaban terverifikasi
1
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia