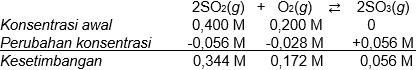Iklan
Pertanyaan
Perhatikan sistem reaksi kesetimbangan antara belerang dioksida dengan oksigen membentuk belerang trioksida berikut: SO 2 ( g ) + O 2 ( g ) → SO 3 ( g ) Anggaplah bahwa sebanyak 0 , 400 mol SO 2 dan 0 , 200 mol O 2 diinjeksikan ke dalam wadah tertutup 1,00 L. Ketika kesetimbangan tercapai, ternyata terbentuk 0 , 056 mol gas SO 3 . Reaksi tidak berangsung sempuma. (a) Berapakah konsentrasi masing-masing gas setelah tercapai kesetimbangan? (b) Gambarkan diagram reaksi yang terjadi berdasarkan perubahan konsentrasi sebagai fungsi waktu .
Perhatikan sistem reaksi kesetimbangan antara belerang dioksida dengan oksigen membentuk belerang trioksida berikut:
Anggaplah bahwa sebanyak dan diinjeksikan ke dalam wadah tertutup 1,00 L. Ketika kesetimbangan tercapai, ternyata terbentuk gas . Reaksi tidak berangsung sempuma.
(a) Berapakah konsentrasi masing-masing gas setelah tercapai kesetimbangan?
(b) Gambarkan diagram reaksi yang terjadi berdasarkan perubahan konsentrasi sebagai fungsi waktu .
Iklan
S. Lubis
Master Teacher
Mahasiswa/Alumni Universitas Sumatera Utara
3
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia