Iklan
Pertanyaan
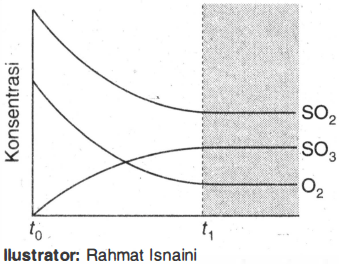
Perhatikan grafik berikut! Berdasarkan grafik tersebut, kesetimbangan tercapai jika ....
Perhatikan grafik berikut!
Berdasarkan grafik tersebut, kesetimbangan tercapai jika ....
pada konsentrasi pereaksi dan hasil reaksi tidak berubah lagi terhadap waktu
reaksi berlangsung dalam dua arah dengan laju yang berbeda
dan bereaksi dan mulai terbentuk produk berupa
sebagian mulai terurai kembali menjadi dan
pada konsentrasi dan menurun
Iklan
BR
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
2
4.7 (9 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia