Iklan
Pertanyaan
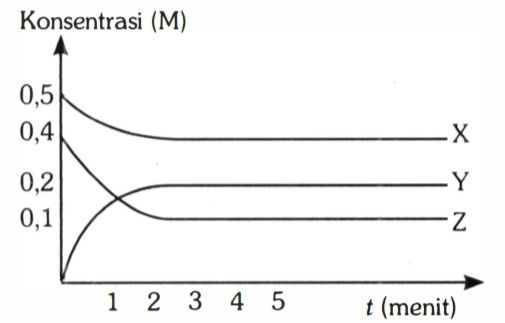
Berikut ini kurva perubahan konsentrasi gas A, B, dan C terhadap waktu hingga terjadi reaksi kesetimbangan pada temperatur tertentu. Jika pada menit ke-3 ditambahkan X, maka ....
Berikut ini kurva perubahan konsentrasi gas A, B, dan C terhadap waktu hingga terjadi reaksi kesetimbangan pada temperatur tertentu.
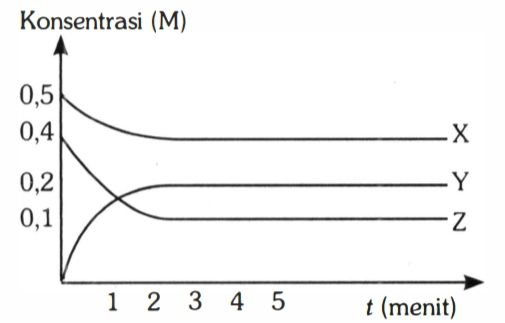
Jika pada menit ke-3 ditambahkan X, maka ....
kesetimbangan bergeser ke arah reaktan
X bertambah
Y bertambah
Z bertambah
tidak terjadi pergeseran kesetimbangan
Iklan
EB
E. Bintang
Master Teacher
Mahasiswa/Alumni Universitas Negeri Yogyakarta
Jawaban terverifikasi
2
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia