Iklan
Pertanyaan
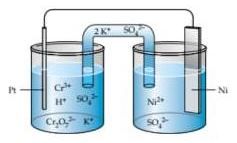
Perhatikan sel galvani berikut: Identifikasi katoda dan anoda Tuliskan reaksi sel! Tuliskan notasi sel!
Perhatikan sel galvani berikut:
- Identifikasi katoda dan anoda
- Tuliskan reaksi sel!
- Tuliskan notasi sel!
Iklan
BR
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
4
4.6 (13 rating)
FP
Febe Priskila Parinding
membantu. tapi bukannya ion selalu berada di tengah²? di dekat jembatan garam.. knp itu beda?
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia