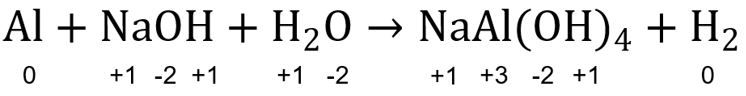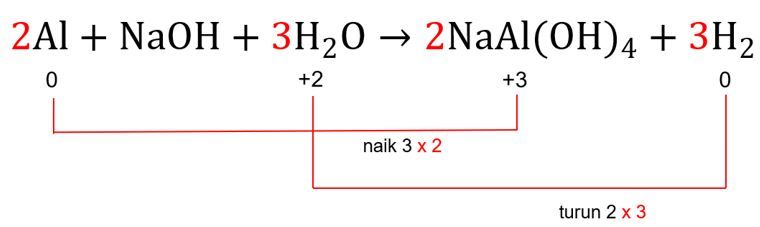Langkah PERTAMA: tentukan biloks setiap unsur yang menyusun senyawa-senyawa dalam persamaan reaksi.
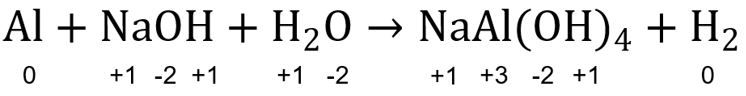
Biloks ruas kiri: Al = 0, Na = +1, O = -2, H = +1
Biloks ruas kanan: Na = +1, Al = +3, O = -2, H = +1,  = 0
= 0
Langkah KEDUA: mengidentifikasi unsur yang mengalami perubahan biloks.
Pada reaksi ini, biloks unsur Al naik dari 0 menjadi +3. Kemudian, biloks unsur H turun dari +1 menjadi 0.
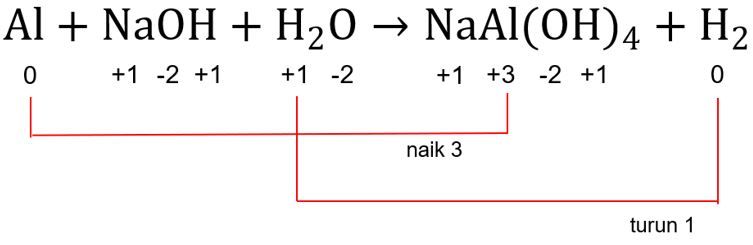
Langkah KETIGA: menghitung total biloks dari unsur-unsur yang mengalami perubahan biloks.
Caranya adalah biloks unsur dikalikan dengan jumlah unsur (dilihat dari indeks atau koefisien unsur).

Karena indeks dan koefisien unsur Al di kiri reaksi sama dengan di kanan reaksi (sama-sama 1), total biloks Al = biloks unsurnya (total biloks Al di ruas kiri = 0, total biloks Al di ruas kanan = +3).
Indeks unsur H di kiri reaksi = 2, sehingga total biloks H di ruas kiri:

Biloks molekul  di ruas kanan = 0
di ruas kanan = 0
Langkah KEEMPAT: menghitung total perubahan biloks.
Biloks unsur Al naik dari 0 menjadi +3, total kenaikannya adalah 3.
Biloks  turun dari +2 menjadi 0, total penurunannya adalah 2.
turun dari +2 menjadi 0, total penurunannya adalah 2.
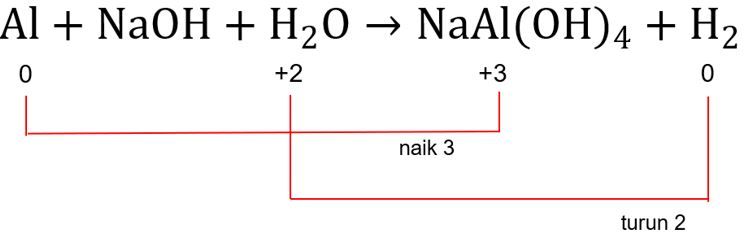
Langkah KELIMA: menyamakan total perubahan biloks pada reaksi.
Sebelumnya sudah diketahui bahwa total kenaikan biloks Al adalah 3, sedangkan total penurunan biloks  adalah 2. Agar total perubahan biloksnya sama, maka kita cari kelipatan terkecil yang sama antara 3 dan 2, yaitu 6. Maka dari itu, kenaikan biloks Al kita kalikan 2, sedangkan penurunan biloks
adalah 2. Agar total perubahan biloksnya sama, maka kita cari kelipatan terkecil yang sama antara 3 dan 2, yaitu 6. Maka dari itu, kenaikan biloks Al kita kalikan 2, sedangkan penurunan biloks  kita kalikan 3. Agar total perubahan biloksnya sama-sama menjadi 6.
kita kalikan 3. Agar total perubahan biloksnya sama-sama menjadi 6.
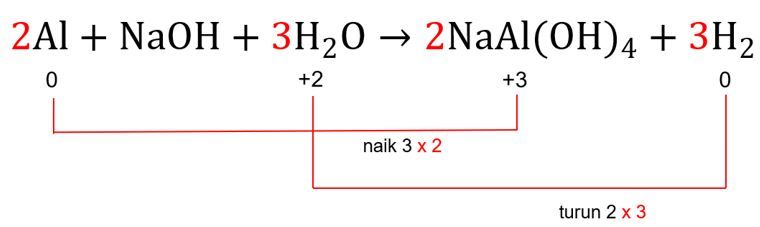
Angka faktor pengali 2 akan menjadi pengali koefisien dari zat yang mengandung unsur Al, sedangkan angka faktor pengali 3 akan menjadi pengali koefisien dari zat yang mengandung  .
.
Langkah KEENAM: menyamakan jumlah unsur yang belum sama (selain oksigen dan hidrogen)
Pada reaksi ini, jumlah unsur yang belum sama adalah unsur Na. Pada ruas kiri terdapat 1 atom Na, sedangkan di ruas kanan terdapat 2 atom Na. Agar jumlah atom Na sama, maka NaOH di ruas kiri kita kalikan 2.

Langkah KETUJUH: menyamakan jumlah unsur oksigen dan hidrogen, pastikan semua unsur jumlahnya sudah sama di ruas kiri dan kanan.
Di ruas kiri jumlah atom H ada 8, sedangkan di ruas kanan jumlah atom H ada 14. Supaya sama,  di ruas kiri kita ubah koefisiennya menjadi 6.
di ruas kiri kita ubah koefisiennya menjadi 6.

Penyetaraan reaksi tersebut dalam suasana basa yang tepat adalah sebagai berikut.

Jadi, jawaban yang tepat adalah opsi B.