Iklan
Pertanyaan
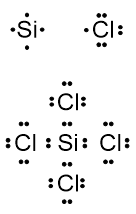
Nomor atom silikon dan klor berturut-turut adalah 14 dan 17. Jika silikon dan klor membentuk senyawa, maka molekul senyawa yang dihasilkan... bersifat nonpolar mempunyai satu pasang elektron bebas pada atom pusatnya berbentuk tetrahedral mempunyai satu ikatan kovalen koordinasi (SOAL SBMPTN 2015)
Nomor atom silikon dan klor berturut-turut adalah 14 dan 17. Jika silikon dan klor membentuk senyawa, maka molekul senyawa yang dihasilkan ...
- bersifat nonpolar
- mempunyai satu pasang elektron bebas pada atom pusatnya
- berbentuk tetrahedral
- mempunyai satu ikatan kovalen koordinasi
(SOAL SBMPTN 2015)
1, 2, dan 3 SAJA yang benar.
1 dan 3 SAJA yang benar.
2 dan 4 SAJA yang benar.
HANYA 4 yang benar.
SEMUA pilihan benar.
Iklan
BR
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
1
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia