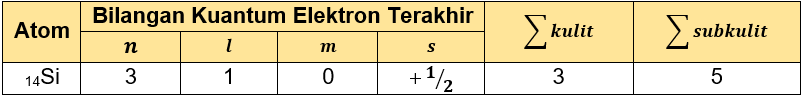
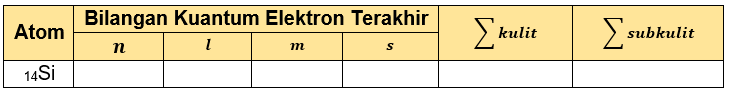
Dalam penentuan keempat bilangan kuantum, diperlukan untuk menentukan elektron terakhir dari konfigurasi elektron terlebih dahulu. Setelah itu elektron terakhir dapat digunakan untuk menentukan bilangan kuantumnya. Terdapat empat jenis bilangan kuantum yaitu:
- Bilangan kuantum utama (n), yang menunjukkan kulit atom.
- Bilangan kuantum azimuth (l), yang menunjukkan subkulit atom.
- Bilangan kuantum magnetik (m), yang menunjukkan jumlah orbital.
- Bilangan kuantum spin (s), yang menunjukkan orientasi elektron terhadap medan magnet di sekitarnya.
Berdasarkan keterangan tersebut, maka:
Konfigurasi elektron 14Si adalah
1s22s22p63s23p2, elektron terakhirnya adalah 3p2. Berdasarkan konfigurasi elektron maka jumlah subkulitnya adalah 5.
Bilangan kuantum 3p2
Bilangan kuantum utama atau n= 3, bilangan kuantum utama menunjukkan jumlah kulit. Jadi jumlah kulitnya adalah 3.
Bilangan kuantum azimuth atau l= 1, karena berada pada subkulit "p". Bilangan kuantum azimuth menunjukkan jumlah subkulit, sehingga jumlah subkulitnya adalah 1.
Bilangan kuantum magnetik dan azimuth:
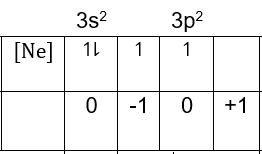
Elektron terakhir ada pada subkulit 3p orbital "0" dengan arah ke atas, maka nilai:
m= 0 dan s= +21
Jadi, jawaban yang benar adalah: