Iklan
Pertanyaan
Kalsium oksida bereaksi dengan gas karbon dioksida membentuk kalsium karbonat menurut persamaan kimia berikut: CaO ( s ) + CO 2 ( g ) → CaCO 3 ( s ) Jika 0,89 gram CaO dan 0,74 gram CO 2 direaksikan, tentukan: pereaksi pembatas, dan massa CaCO 3 yang dihasilkan.
Kalsium oksida bereaksi dengan gas karbon dioksida membentuk kalsium karbonat menurut persamaan kimia berikut:
Jika 0,89 gram dan 0,74 gram direaksikan, tentukan:
- pereaksi pembatas, dan
- massa yang dihasilkan.
Iklan
BR
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
1
4.0 (8 rating)
AR
AZKIA RAISA FADILLA
Pembahasan lengkap banget
CM
Crystalia Mayasari Sitio
Ini yang aku cari!
AA
Atsal Aus Ghussan
Pembahasan lengkap banget
AN
Akhsa Nareswara
Pembahasan tidak menjawab soal
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia



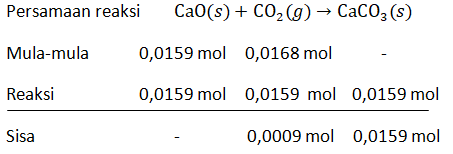 .
.











