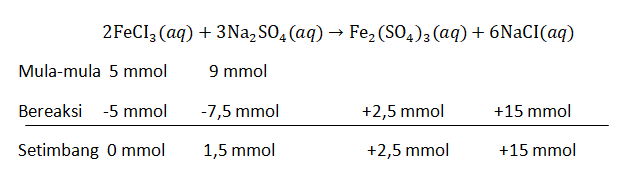Iklan
Pertanyaan
Sebanyak 10 ml larutan FeCI 3 0,5 M direaksikan dengan 45 ml larutan natrium sulfat 0,2 M menurut reaksi berikut. FeCI 3 ( a q ) + Na 2 SO 4 ( a q ) → Fe 2 ( SO 4 ) 3 ( a q ) + NaCI ( a q ) (reaksi belum setara) Berapakah jumlah Na 2 SO 4 yang tidak habis bereaksi?
Sebanyak 10 ml larutan 0,5 M direaksikan dengan 45 ml larutan natrium sulfat 0,2 M menurut reaksi berikut.
(reaksi belum setara)
Berapakah jumlah yang tidak habis bereaksi?
Iklan
GS
G. Suprobo
Master Teacher
Mahasiswa/Alumni Institut Pertanian Bogor
Jawaban terverifikasi
3
4.2 (5 rating)
M
Master
Makasih Bantu banget
ZJ
Zahra Jannah
Mudah dimengerti Pembahasan lengkap banget Makasih ❤️ Ini yang aku cari! Bantu banget
L
Lukita
Jawaban tidak sesuai Pembahasan tidak menjawab soal
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia