Keberadaan ligan pada ion kompleks ini memegang peran penting dalam hal geometri ion kompleks. Hal ini dapat terjadi, karena adanya perbedaan kekuatan ligan. Ligan itu dibedakan menjadi 2, ada ligan kuat dan juga ada ligan lemah.
Berikut ini adalah urutan kekuatannya,
Ligan kuat : 
Ligan lemah : 
Terlihat disini bahwa ligan CN- merupakan ligan kuat.
Untuk ligan kuat seperti ligan CN- dapat terjadi dua kemungkinan,
- Jika jumlah elektron yang tidak berpasangan pada atom pusat berjumlah genap, maka akan mendesak elektron tersebut untuk berpasangan.
- Jika jumlah elektron yang tidak berpasangan nya ganjil, maka nanti elektron ini mengalami eksitasi ke orbital lain yang kosong.
Disini terdapat atom pusat Cu dengan nomor atom 29, dan bila dihitung, bilangan oksidasi atom pusatnya adalah +2.
Muatan ion kompleks = muatan ligan + biloks atom pusat
-2 = 4x(-1) + biloks Cu
Biloks Cu = +2
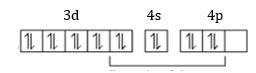
Berikut ini adalah konfigurasi elektron dan diagram orbitalnya :

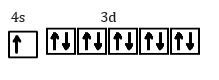

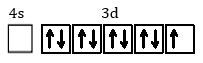
Pada ion Cu2+ ini memiliki jumlah elektron yang tidak berpasangan nya ganjil, yaitu sebanyak 1 elektron. Maka nanti elektron ini mengalami eksitasi ke orbital lain yang kosong, seperti ini:

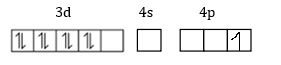
Selanjutnya, terdapat 1 orbital kosong pada orbital 3d. Sehingga nanti 4 pasangan elektron dari ligan CN- yang merupakan ligan kuat akan menempati orbital kosong yang dimiliki oleh ion Cu2+. Keempat orbital itu adalah 1 orbital 3d, 1 orbital 4s dan 2 orbital 4p, dan nantinya akan terjadi hibridisasi sehingga akan membentuk orbital hibrida dsp2, dimana orbital hibrida ini memiliki geometri segiempat planar.