Pada hibridisasi ion kompleks, atom pusat harus menyiapkan orbital kosong yang akan ditempati oleh pasangan elektron bebas dari ligan. Ion [Ag(NH3)2]+ menunjukkan bahwa atom pusatnya adalah Ag dengan nomor atom 47. Jika dibuat konfigurasi elektron dan diagram orbitalnya, hasilnya adalah sebagai berikut.
47Ag=[36Kr] 5s1 4d10
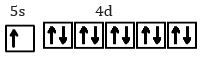
Ion kompleks ini memiliki NH3 sebagai ligan. Muatan NH3 adalah 0.
muatanion kompleks+1biloks Ag===muatanligan+biloks atom pusat2x(0)+biloks Ag+1
Ion pusatnya adalah ion Ag+ (lepas 1 elektron). Konfigurasi elektron dan diagram orbitalnya adalah sebagai berikut.
47Ag=[36Kr] 4d10 5s0 5p0
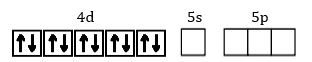
Pada ion kompleks [Ag(NH3)2]+, ion Ag+ menerima 2 pasang elektron bebas dari NH3. Oleh karena itu, Ag+ harus menyiapkan 2 orbital kosong untuk menerima 2 pasang elektron koordinasi dari NH3. Orbital kosong yang digunakan adalah 5s dan 5p.
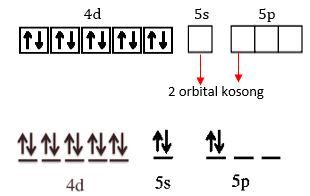
Oleh karena tingkat energi 5s dan 5p berbeda (5s lebih rendah dari 5p), kedua orbital terhibridisasi sehingga membentuk orbital hibrida sp yang memiliki geometri linear.
Jadi, jawaban yang benar adalah B.


















