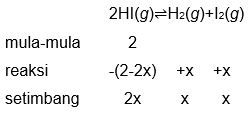Iklan
Pertanyaan
Gas HI sebanyak 2 mol dalam wadah 5 L terurai sesuai persamaan reaksi: 2 HI ( g ) ⇌ H 2 ( g ) + I 2 ( g ) Jika pada saat setimbang terdapat perbandingan mol HI : I 2 = 2 : 1 , tetapan kesetimbangan dari reaksi ini adalah . . . .
Gas HI sebanyak 2 mol dalam wadah 5 L terurai sesuai persamaan reaksi:
Jika pada saat setimbang terdapat perbandingan mol HI : = 2 : 1 , tetapan kesetimbangan dari reaksi ini adalah . . . .
0,1
0,25
0,5
0,75
1
Iklan
SH
S. Hidayati
Master Teacher
Mahasiswa/Alumni Universitas Indonesia
Jawaban terverifikasi
9
4.5 (7 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia