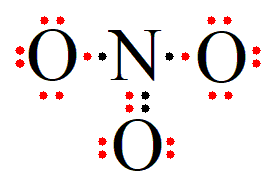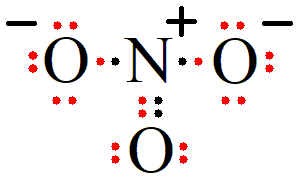Langkah 1: Tentukan jumlah elektron valensi masing-masing atom dan jumlahnya.

Langkah 2: Tentukan jumlah elektron valensi tiap atom dan jumlahnya jika memenuhi aturan oktet

Langkah 3: Menghitung selisih elektron valensi oktet dengan elektron valensi sebenarnya
Selisih elektron valensi = 32 – 23 = 9 elektron valensi
Langkah 4: menghitung jumlah ikatan dengan membagi dua selisih elektron valensi
Agar jumlah ikatan dapat dibagi dua maka 1 elektron tidak digunakan dalam pembuatan struktur lewis artinya 1 elektron ini dilepaskan oleh atomnya. Dengan demikian elektron selisih adalah 8.
Jumlah ikatan = 8 : 2 = 4 ikatan
Langkah 5: Menggambarkan struktur lewis dengan 4 ikatan kimia berdasarkan aturan oktet.
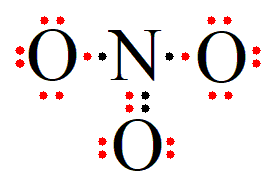
Langkah 6: Menentukan atom manakah yang bermuatan.
Terlihat bahwa atom N kekurangan elektron valensi. Seharusnya elektron valensi atom N adalah 5, sedangkan pada struktur lewis hanya memiliki 4 elektron valensi. Artinya elektron yang tidak digunakan dalam pembuatan struktur lewis (elektron yang dilepas) merupakan elektron yang dimiliki atom N. Dengan demikian atom N bermuatan +1. Sedangkan pada atom O terlihat bahwa dua buah atom O yang ada di kanan dan kiri atom C memiliki kelebihan elektron valensi. Seharusnya atom O hanya memiliki 6 elektron valensi sedangkan dari strutur lewis terlihat atom O memiliki 7 elektron valensi. Jadi dua buat atom O tersebut masing-masing bermuatan -1 dan muatan totalnya adalah -2. Sehingga struktur lewisnya adalah
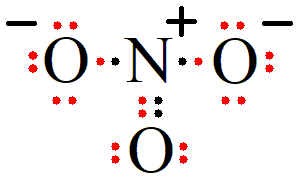
Langkah 7: Menentukan muatan formal





Dengan demikian, struktur lewis dari  adalah yang tertera diatas dan muatan formal dari struktur
adalah yang tertera diatas dan muatan formal dari struktur  lewis adalah -1.
lewis adalah -1.