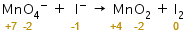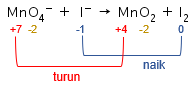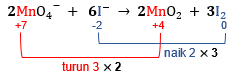Penyetaraan reaksi redoks dengan metode biloks dalam suasana basa adalah sebagai berikut.
Langkah 1: menghitung biloks setiap unsur.
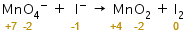
Langkah 2: mengidentifikasi unsur yang mengalami perubahan biloks.
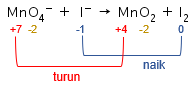
Langkah 3: menyamakan jumlah unsur yang mengalami perubahan biloks, yaitu unsur Mn dan I.

Langkah 4: menghitung total biloks unsur yang mengalami perubahan biloks dengan cara dikalikan dengan indeks atau koefisien unsur.
Jumlah unsur Mn pada ruas kiri dan kanan adalah 1 sehingga total biloks Mn dikalikan 1. Sedangkan jumlah unsur I pada ruas kiri dan kanan adalah 2, maka total biloks unsur I dikalikan 2.

Langkah 5: menghitung total perubahan biloks pada reaksi.
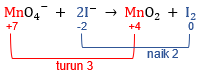
Langkah 6: menyamakan total perubahan biloks pada reaksi.
Kenaikan biloks unsur I adalah 2, sedangkan penurunan biloks unsur Mn adalah 3 Agar total perubahan biloksnya sama, maka cari kelipatan terkecil antara 2 dan 3, yaitu 6. Maka, kenaikan biloks unsur I dikalikan 3 dan penurunan biloks unsur Mn dikalikan 2.
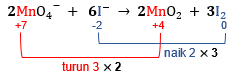
Angka faktor pengali 2 menjadi pengali koefisien dari zat yang mengandung unsur Mn, sedangkan angka faktor pengali 3 menjadi pengali koefisien dari zat yang mengandung unsur I.
Langkah 7: menyamakan jumlah muatan dengan menambah ion  pada ruas yang muatannya lebih besar.
pada ruas yang muatannya lebih besar.
Muatan pada ruas kiri adalah  8, sedangkan muatan pada ruas kanan adalah 0. Maka, tambahkan 8 ion
8, sedangkan muatan pada ruas kanan adalah 0. Maka, tambahkan 8 ion  pada ruas kanan sehingga persamaan reaksinya menjadi
pada ruas kanan sehingga persamaan reaksinya menjadi

Langkah 8: menyamakan jumlah oksigen dengan menambahkan  pada ruas yang kekurangan oksigen.
pada ruas yang kekurangan oksigen.
Terdapat 8 atom O pada ruas kiri dan 12 atom O pada ruas kanan. Artinya, di ruas kiri masih kurang 4 atom O sehingga perlu menambahkan 4  . Persamaan reaksinya menjadi
. Persamaan reaksinya menjadi

Langkah 9: memeriksa kembali reaksi setara.

Jumlah unsur dan muatan pada kedua ruas sudah sama, yaitu Mn = 2, I = 6, H = 8, O = 12, dan jumlah muatan =  8.
8.
Jadi, jawaban yang tepat adalah A.