Iklan
Pertanyaan
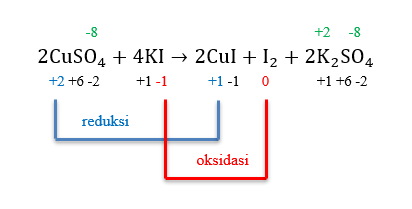
Diketahui reaksi: 2 CuSO 4 + 4 KI → 2 CuI + I 2 + 2 K 2 SO 4 Jika reaksi tersebut merupakan reaksi redoks, tentukan oksidator, reduktor, hasil oksidasi, dan hasil reduksi!
Diketahui reaksi:
Jika reaksi tersebut merupakan reaksi redoks, tentukan oksidator, reduktor, hasil oksidasi, dan hasil reduksi!
Iklan
SL
S. Lubis
Master Teacher
Jawaban terverifikasi
4
4.9 (15 rating)
Nz
Nayla zahirra Arjani
Makasih ❤️
TS
TIARA SITA DEWI
Pembahasan lengkap banget Ini yang aku cari! Mudah dimengerti Bantu banget Makasih ❤️
EN
Esterina Nenabu
Pembahasan lengkap banget
LE
Lilis Erna
Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia