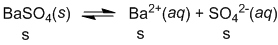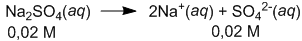Iklan
Pertanyaan
Diketahui Ksp BaSO 4 = 1 , 1 × 1 0 − 10 , maka kelarutan BaSO 4 dalam larutan Na 2 SO 4 0,02 M adalah … mol L –1 .
Diketahui Ksp = , maka kelarutan dalam larutan 0,02 M adalah … mol L–1.
Iklan
EB
E. Bintang
Master Teacher
Mahasiswa/Alumni Universitas Negeri Yogyakarta
Jawaban terverifikasi
1
4.7 (4 rating)
n
naurellian
Mudah dimengerti
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia