Iklan
Pertanyaan
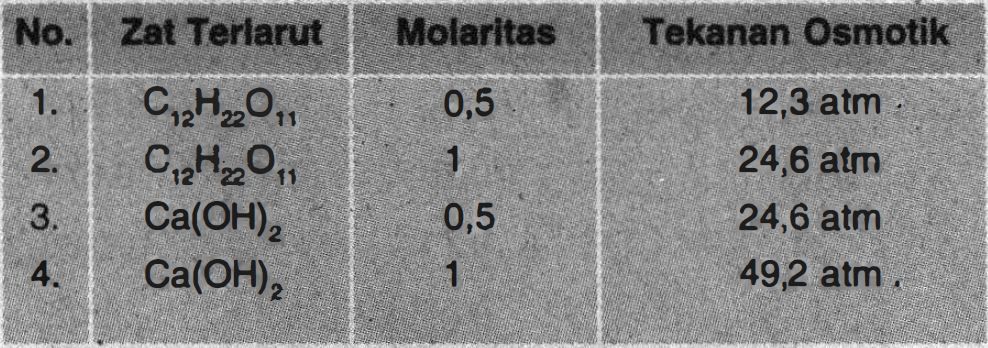
Data percobaan tentang tekanan osmotik empat larutan pada suhu 2 7 ∘ C disajikan dalam tabel berikut. Pada konsentrasi yang sama, larutan C 12 H 22 O 11 dan Ca ( OH ) 2 memiliki tekanan osmotik yang berbeda. Hal ini disebabkan kedua larutan ....
Data percobaan tentang tekanan osmotik empat larutan pada suhu disajikan dalam tabel berikut.
Pada konsentrasi yang sama, larutan dan memiliki tekanan osmotik yang berbeda. Hal ini disebabkan kedua larutan ....
menghasilkan jumlah partikel yang tidak sama
mempunyai molekul yang tidak sama besarnya
mempunyai derajat ionisasi yang sama
sama-sama larutan non elektrolit
sama-sama larutan elektrolit
Iklan
SL
S. Lubis
Master Teacher
Jawaban terverifikasi
4
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia